아이오딘화 질소
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
아이오딘화 질소(NI3)는 질소와 요오드의 화합물로, 삼각뿔형 구조를 가지며 매우 불안정하여 작은 충격에도 폭발하는 특성을 지닌다. 요오드와 암모니아의 반응으로 생성되며, 무수 암모니아 조건에서 NI3 · (NH3)5, 온도 상승 시 NI3 · NH3 부착물을 형성한다. 순수한 NI3는 붕소 질화물과 플루오린화 요오드의 반응으로 얻을 수 있다. NI3는 큰 입체 변형으로 인해 분해가 쉽게 일어나며, 질소 기체와 요오드로 분해된다. 극심한 충격 감도로 인해 상업적 가치는 없으며, 고등학교 화학 실험에서 시연용으로 사용되기도 한다. 폭발 후에는 요오드 얼룩이 남으며, 티오황산 나트륨 용액으로 제거할 수 있다.
더 읽어볼만한 페이지
- 질소 화합물 - 아마이드
아마이드는 카복실산 유도체로 카보닐기에 질소 원자가 결합된 아마이드기를 가지며, 약한 염기성, 부분적인 이중 결합 특성, 수소 결합 형성 능력으로 인해 다양한 화학 반응 및 단백질 구조 형성에 중요한 역할을 한다. - 질소 화합물 - 사이안화물
사이안화물은 탄소와 질소의 삼중 결합으로 이루어진 시안화 이온을 포함하는 화합물로, 자연적으로 생성되기도 하며 산업적으로 활용되지만, 독성이 강하여 인체에 치명적일 수 있다. - 아이오딘화물 - 아이오딘화 칼륨
아이오딘화 칼륨은 의학, 산업, 영양 등 다양한 분야에서 활용되는 이온 화합물로, 특히 방사성 요오드 노출 시 갑상선 보호 효과와 요오드 결핍 예방에 사용된다. - 아이오딘화물 - 아이오딘화 암모늄
아이오딘화 암모늄은 암모니아와 아이오드화 수소산의 반응으로 생성되는 화합물로, 요오드 결핍 치료제 및 비닐 설폰 제조와 같은 유기 반응에 사용되며, 과산화 수소와 함께 케톤 및 방향족 화합물을 아이오딘화하는 친환경적인 유기 합성법에 응용된다. - 폭약 - 오존화물
오존화물은 굽은 형태의 O₃⁻ 음이온을 포함하는 이온 화합물로, 알칼리 금속 또는 알칼리 토금속과 오존의 반응 등으로 생성되며, 화학적 산소 발생기나 일중항 산소 생성 중간체로 연구되지만, 분자 오존화물은 불안정하여 트리옥솔란으로 전환되거나 물과 반응하여 분해된다. - 폭약 - 피크르산
피크르산은 쓴맛을 내는 노란색 결정으로, 다양한 용도로 사용되며 충격과 마찰에 민감하여 안전에 유의해야 하는 페놀류의 일종이다.
2. 구조
질화 삼요오드(Nitrogen triiodide영어)는 암모니아와 마찬가지로 삼각뿔형 분자 구조(C3v 분자 대칭)를 갖는다.[4] 1990년 무암모니아 경로로 순수한 NI3가 처음 제조되었으며, 라만 분광법으로 특성화되었다. 질화 붕소와 일불화 요오드를 −30 °C에서 삼염화플루오로메탄 내에서 반응시켜 낮은 수율로 순수한 NI3를 얻을 수 있다.[3]
NI3와 NI3 · NH3의 불안정성은 질소 원자 주위에 3개의 큰 요오드 원자가 가까이 있어 발생하는 입체 변형 때문이다. 이는 낮은 활성화 에너지를 가지며, N2 생성으로 인해 분해 반응이 더욱 촉진된다.[4] 분해 반응식은 다음과 같다.
일반적으로 요오드와 암모니아를 반응시켜 합성한다. 진한 암모니아 수용액에 요오드를 넣으면 바늘 모양의 요오드화 질소 결정이 석출된다. 이 반응을 무수 암모니아에서 저온으로 수행하면, 처음에 NI3•(NH3)5가 생성된다. 이를 가열하면 이 화합물에서 암모니아가 떨어져 나가 NI3•NH3이 된다. 이 부가물은 1812년 베르나르 쿠르투아가 처음 보고했고, 1905년 실버라드(Silberrad)가 조성을 결정했다[12].
아이오딘화 질소는 극도로 충격에 민감하여 실용적인 상업적 가치가 없다. 저장, 운송 및 통제된 폭발이 불가능하기 때문이다.[4] 고등학교 화학 실험에서 시연 목적으로 소량 합성되기도 한다.[7] 화합물의 민감성을 강조하기 위해 깃털로 건드려 폭발시키거나, 아주 작은 기류, 레이저 빛, 또는 기타 움직임으로도 폭발을 일으킬 수 있다.[8] 알파 입자 및 핵분열 생성물에 노출되었을 때 폭발하는 유일한 화학 폭발 물질로도 알려져 있다.[8]
[1]
문서
per analogiam
일반적으로 "질화 삼요오드"라고 불리는 물질은 요오드와 암모니아의 반응으로 만들어진다. 무수 암모니아 조건, 저온에서 반응시키면 NI3 · (NH3)5가 생성되고, 온도가 상승하면 암모니아가 떨어져 나가 NI3 · NH3 부착물이 생성된다.[5] 이 부착물은 1812년 베르나르 쿠르투아가 처음 보고했고, 1905년 오스왈드 실버라드가 그 조성을 결정했다.[5] NI3 · NH3 고체 상태에서는 -NI2-I-NI2-I-NI2-I- 사슬 구조를 가지며, 암모니아 분자는 사슬 사이에 위치한다.[6]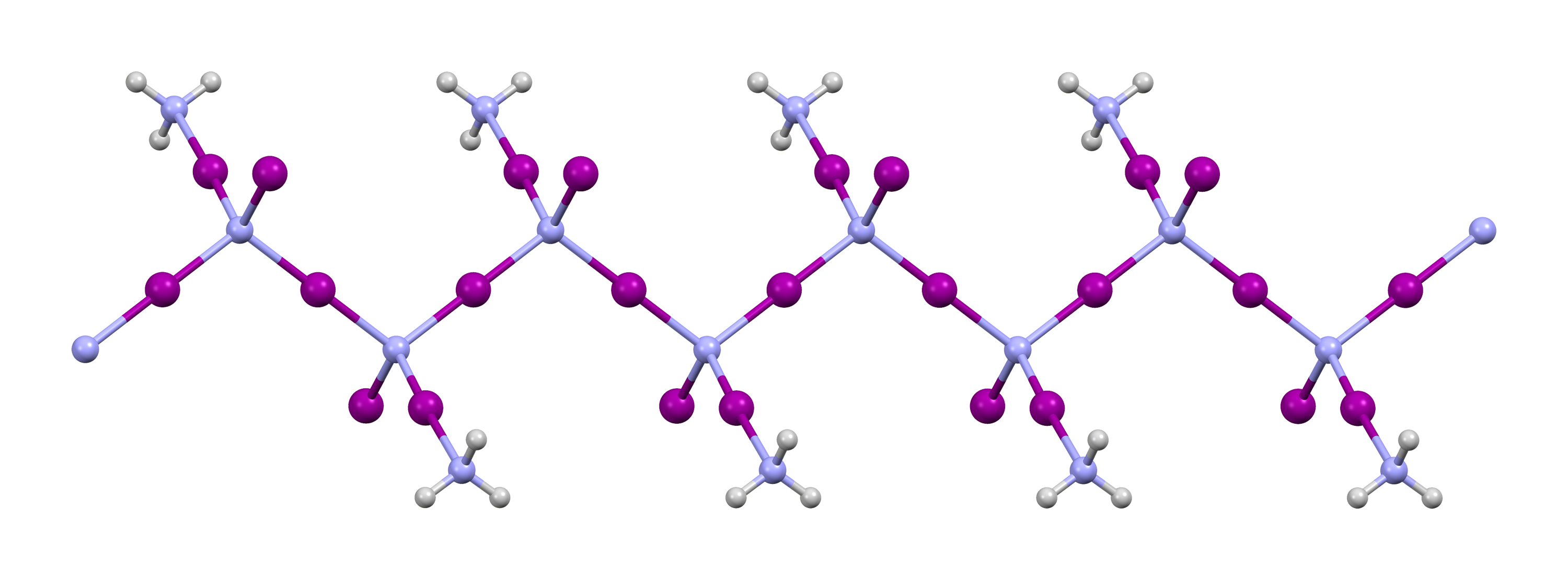
3. 분해 및 폭발성
:2 NI3 (s) → N2 (g) + 3 I2 (g) (−290 kJ/mol)
건조 상태에서는 접촉 폭발성이 매우 강하며, 깃털, 약한 기류, 레이저 빛, 알파 입자, 핵분열 생성물 등에 의해서도 폭발할 수 있다.[7][8] 폭발 후에는 요오드로 인한 주황색-보라색 얼룩이 남으며, 티오황산 나트륨 용액으로 제거하거나 요오드가 승화되도록 하여 제거할 수 있다.[4]
건조 상태에서 분해 반응식은 다음과 같다.[4]
: 8 NI3 · NH3 → 5 N2 + 6 NH4I + 9 I2
4. 합성
1990년에는 암모니아를 사용하지 않고 합성하여 X선 결정 구조 해석을 진행했다. 질화 붕소와 플루오린화 요오드를 트리클로로플루오로메탄에서 -30°C로 반응시켜, 낮은 수율로 NI3을 얻었다[10].
5. 이용
화학 실험 수업에서 소량 합성이 이루어지는 경우가 있는데, 삼아이오딘화 질소가 충격에 민감하다는 것을 보여주기 위해 깃털 끝으로 만져 폭발을 일으키는 경우가 많지만, 기류가 닿거나 조금만 움직여도 폭발하는 경우가 있다([http://www.youtube.com/watch?v=2KlAf936E90 실험 영상]). 또한, 삼아이오딘화 질소는 알파선이나 중성자선에 노출되어도 폭발한다.
NI3•NH3가 폭발하면 주황색에서 보라색 얼룩이 남는데, 이는 티오황산 나트륨 용액으로 제거할 수 있다.
영국의 과학 오락 프로그램 "Brainiac: Science Abuse"에서는 "피터 로건의 폭발 페이스트 (Peter Logan's Exploding Paste)"로 소개되었다. 안전을 위해 자세한 제조법은 소개되지 않았다.
로버트 A. 하인라인의 소설 『자유 미래 (''Farnham's Freehold'')』에서는, 그 이름의 유래인 휴 파넘 (Hugh Farnham)이 암모니아와 아이오딘으로부터 만든 삼아이오딘화 질소를 폭파약으로 사용했다.
참조
[2]
웹사이트
4. Analytical techniques
http://www.acornuser[...]
[3]
논문
Nitrogen Triiodide
[4]
서적
Inorganic Chemistry
Academic Press
[5]
논문
The Constitution of Nitrogen Triiodide
https://zenodo.org/r[...]
[6]
논문
Die Kristallstruktur von Stickstofftrijodid‐1‐Ammoniak NJ3 · NH3
[7]
서적
Chemical Magic
https://archive.org/[...]
Dover
[8]
논문
Initiation of Explosion by Neutrons, α-Particles, and Fission Products
[9]
문서
窒素のほうがヨウ素よりも電気陰性度が大きいため、定義上はヨウ素の窒化物である。
[10]
논문
Angew. Chem., Int. Ed. Engl.
[11]
서적
Inorganic Chemistry
Academic Press
[12]
논문
On the Constitution of Nitrogen Triiodide.
[13]
문서
per analogiam
[14]
웹사이트
4. Analytical techniques
http://www.acornuser[...]
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com
